辉瑞、BioNTech 为 5-11 岁儿童寻求美国疫苗许可
 路透社消息,辉瑞周四(美国时间)表示,辉瑞公司( PFE.N )和 BioNTech SE 已向美国监管机构授权他们的新冠疫苗紧急用于 5 至 11 岁的儿童,该年龄组的儿童目前不允许注射。
路透社消息,辉瑞周四(美国时间)表示,辉瑞公司( PFE.N )和 BioNTech SE 已向美国监管机构授权他们的新冠疫苗紧急用于 5 至 11 岁的儿童,该年龄组的儿童目前不允许注射。
美国食品和药物管理局外部顾问小组已将其日期定为 10 月 26 日,届时将召开会议并讨论该申请,使这一年龄组的儿童(约 2800 万)有可能开始接受两剂辉瑞/ BioNTech 疫苗。
辉瑞在 Twitter 上写道:“随着美国儿童的新病例继续处于高水平,此次提交是我们针对疫情持续努力的重要一步。”
该疫苗已获得美国 12 至 15 岁青少年的紧急使用授权,并已获得监管机构的全面批准,适用于 16 岁及以上的人群。

辉瑞/BioNTech 疫苗是美国使用的三种疫苗之一,另外还有两剂 Moderna (MRNA.O)疫苗和单剂强生(JNJ.N)疫苗,这两种疫苗都没有获得完全的年龄组的监管批准。
辉瑞/BioNTech 疫苗在幼儿中的快速批准可能有助于缓解未来几周和几个月内潜在的病例激增,因为学校在全国范围内开放,在美国寒冷的天气使活动将在更多在室内进行。如果获得监管授权,两剂辉瑞/BioNTech 疫苗将成为美国 5 至 11 岁儿童可接种的首个疫苗选择。
两家公司于 9 月 20 日表示,辉瑞 / BioNTech 疫苗已在一项有 2268 名参与者的临床试验测试 5 至 11 岁儿童可能会产生的强烈的免疫反应。
这两家制药商还在 2 至 5 岁的儿童和 6 个月至 2 岁的儿童中测试疫苗,预计将在第四季度公布数据。
白宫 疫情响应协调员杰弗里·齐恩茨(Jeffrey Zients)在美国有线电视新闻网(CNN)上说,该疫苗最早可在 11 月推出,等待联邦监管卫生机构的批准。
获得授权后,Zients 说:“我们准备好正在与各州合作,为父母和孩子设置方便的接种地点,包括儿科医生办公室和社区站点。”
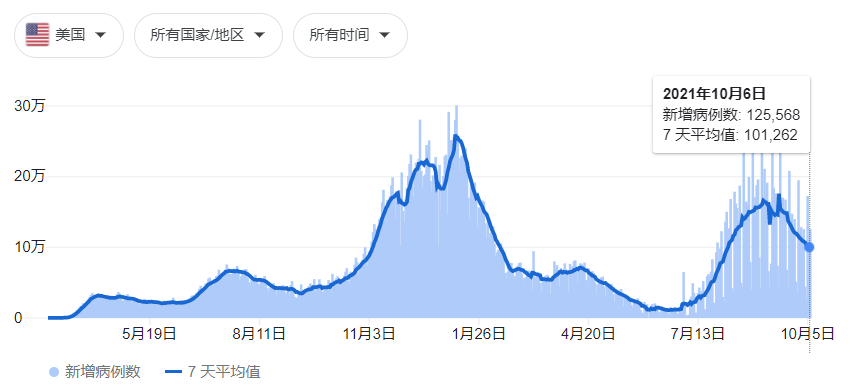
美国在疫情病例和死亡人数方面领先世界。
根据美国儿科学会的数据,儿童目前约占美国所有冠状病毒病例的 27%,住院治疗的比例越来越高。这反映了冠状病毒 Delta 变体在未接种疫苗的人群中的高传染性。
虽然儿童不太容易感染严重的新冠,但他们可以携带病毒并传播给其他人,包括更有可能患上严重疾病的弱势群体。
辉瑞发言人表示,已完成向 FDA 的申请。